- HOME
- 臨床研究 不整脈
基礎・トランスレーショナル研究
不整脈1│不整脈2│血管炎│心不全│血液凝固│その他│循環生理解析グループ
臨床研究
不整脈の臨床研究
不整脈治療は大きく薬物治療と非薬物治療に分けられます。当科の不整脈チームはこのうち非薬物治療を得意としています。年間500症例を超えるカテーテルアブレーションを行っています。なかでも心房細動(特に持続型心房細動)や心室頻拍・心房頻拍などの難治性不整脈に対するアブレーション(経皮的カテーテル心筋焼灼術)、ペースメーカーや植え込み型除細動(ICD)等のデバイス留置患者の感染症・非感染症に対するリード抜去術に関する臨床研究に力を入れています。
カテーテルアブレーション①
心房細動アブレーションに関する臨床研究
研究目的
心房細動は本邦では100万人が罹患していると推定されており、不整脈疾患の中では最も患者数の多い疾患です。心房細動患者は脳梗塞を発症しやすいことはよく知られていますが、心不全も発症しやすく、動悸や労作時息切れなどの症状のある症例では、心房細動を抑える治療(リズムコントロール)が必要となります。抗不整脈薬の効果は不十分であることが多いため、カテーテルアブレーションによる治療が世界的にも増加しており、世界中のカテーテルアブレーション件数の60-70%が心房細動を対象としたものとなっています。 当科では最新の機器を用いてアブレーション治療を行い、新しい機器の効果的な使用方法の開発、数多くの関連施設・連携施設と治療データを共有し、より有効かつ安全な心房細動アブレーション治療のためのエビデンスの構築、新たな治療法の開発を目的として研究を行っています。
研究内容
<心房細動アブレーション後の脳梗塞・出血リスクの評価>
心房細動アブレーションは頻拍発作による症状の緩和が最大の目的の治療になりますが、心房細動発作を抑制することによる脳梗塞リスクの低減も期待されています。また、心房細動の抑制に成功した場合には、一部の患者、特に出血リスクの高い患者では抗凝固薬が中止されることもあります。一方で、抗凝固薬の中止後に心房細動が再発することもあり、そのようなケースの脳梗塞リスクが懸念されます。実臨床において、抗凝固薬を中止するか継続するか決定する際には、臨床データ・エビデンスを参考にする必要がありますが、まだこの問題に関する十分なデータがありません。当科では、心房細動アブレーション後の患者の抗凝固薬内服、心房細動再発有無、脳梗塞、出血イベントを、関連施設と共同で調査しています。なお、本研究は科研費の助成を受けています(科学研究費基盤(C)17K09489)。
<レーザーバルーンアブレーションの肺静脈狭小化リスクの探索>
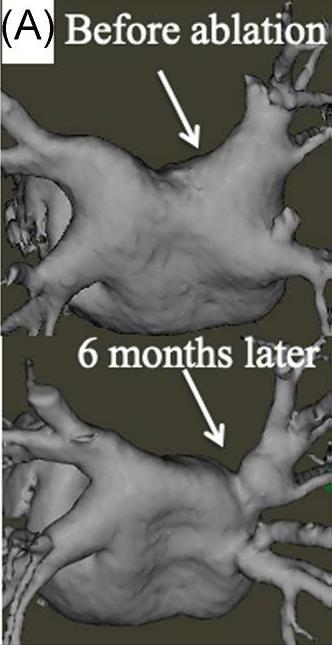
図1:レーザーバルーンアブレーション
前後の肺静脈(文献1より)
心房細動アブレーションには様々な術式がありますが、肺静脈隔離は全ての心房細動患者に行われる基本となる術式です。現在、従来から用いられてきた高周波アブレーションとクライオバルーンの主に2種類の方法があります。それらに加え、2018年よりレーザーバルーンアブレーションが日本で保険収載され、用いられるようになりました。レーザーバルーンアブレーションはクライオバルーンと同様に、高周波アブレーションに比較してカテーテルの操作が簡易で、かつクライオバルーンと異なり、焼灼部位毎にレーザーエネルギーやレーザー照射時間を調整することができるという特徴があります。しかしながら、レーザーはこれまでアブレーション治療に全く用いられたことがないエネルギー源であり、有効性や安全性に関して欧米でのデータしかありませんでした。当科では、本邦で第一例目のレーザーバルーンアブレーションを行い、その後も症例を重ね、レーザーバルーンアブレーションによる肺静脈狭小化をCTで調査し、そのリスクを検討しました。レーザーバルーンを用いて肺静脈隔離を施行した38例のうち、肺静脈閉塞は1例もみとめませんでしたが、無症候性の肺静脈の中等度狭小化を27%の肺静脈にみとめました(図1)。中等度以上の狭小化をみとめた肺静脈は、術前の肺静脈径が大きく、そのためレーザーバルーンが左心房・肺静脈接合部よりも遠位部に入り込み、接合部よりも遠位部が焼灼されていることがわかりました(文献1)。この研究結果より、肺静脈狭窄を避けるためには、特に径の大きい肺静脈において、通電前のレーザーバルーンの位置が重要であることが明らかとなりました。
<持続性心房細動に対するマッピング研究>
心房細動が始まる際には、トリガーと呼ばれる心房細動の最初の不整脈(心房期外収縮)が出現し、その後、心房細動が持続します。心房細動が持続するために必要となる組織は基質(substrate)と呼ばれます。発作性心房細動の90%の症例はトリガーも基質も肺静脈内に存在するため、肺静脈隔離のみで発作を抑制することができます。心房細動が発作性から持続性へと進行すると、トリガーや基質は肺静脈外にも出現します。その結果、持続性心房細動に対しては、肺静脈隔離のみでは30-40%の症例で心房細動の再発をみとめます。これまで持続性心房細動に対しては、肺静脈隔離に加えて、非肺静脈組織を起源とするトリガーを標的としたアブレーションが最も一般的な術式でしたが、トリガーを再現性高く誘発する方法がないため、アブレーション治療成績には限界がありました。そこで、当科では持続性心房細動の基質を探す(マッピング)方法の臨床応用に取り組んでいます。これまでの研究により、心房細動中には心房内のある一点から興奮が繰り返し出現し、周囲に放射状に広がるfocal sourceと呼ばれる現象や、心房内の小さい領域を興奮が旋回する(rotation)ことがわかっていましたが、電極カテーテルにより得られる電気的情報の解析に時間を要するため、アブレーション治療への応用が困難でした。当科では、CARTO3®という3Dマッピングシステムの心房細動の興奮様式自動解析のための新しい機能であるCARTOFINDERを用いて研究を行っています。CARTOFINDERは2019年秋からヨーロッパ、2020年1月から本邦でも臨床使用されていますが、当科では臨床使用が承認される前から、アブレーション中に得られたデータを治療後にCARTOFINDERを用いて解析しました。肺静脈隔離が終わった持続性心房細動の症例では、興奮旋回(rotation)は43%の症例、focal sourceは全例でみとめました。また、最もfocal sourceを高頻度にみとめた部位は左心耳と右心耳で、両心耳のfocal sourceが持続性心房細動の基質として重要な役割を果たしていることが示唆されました(図2、文献2)
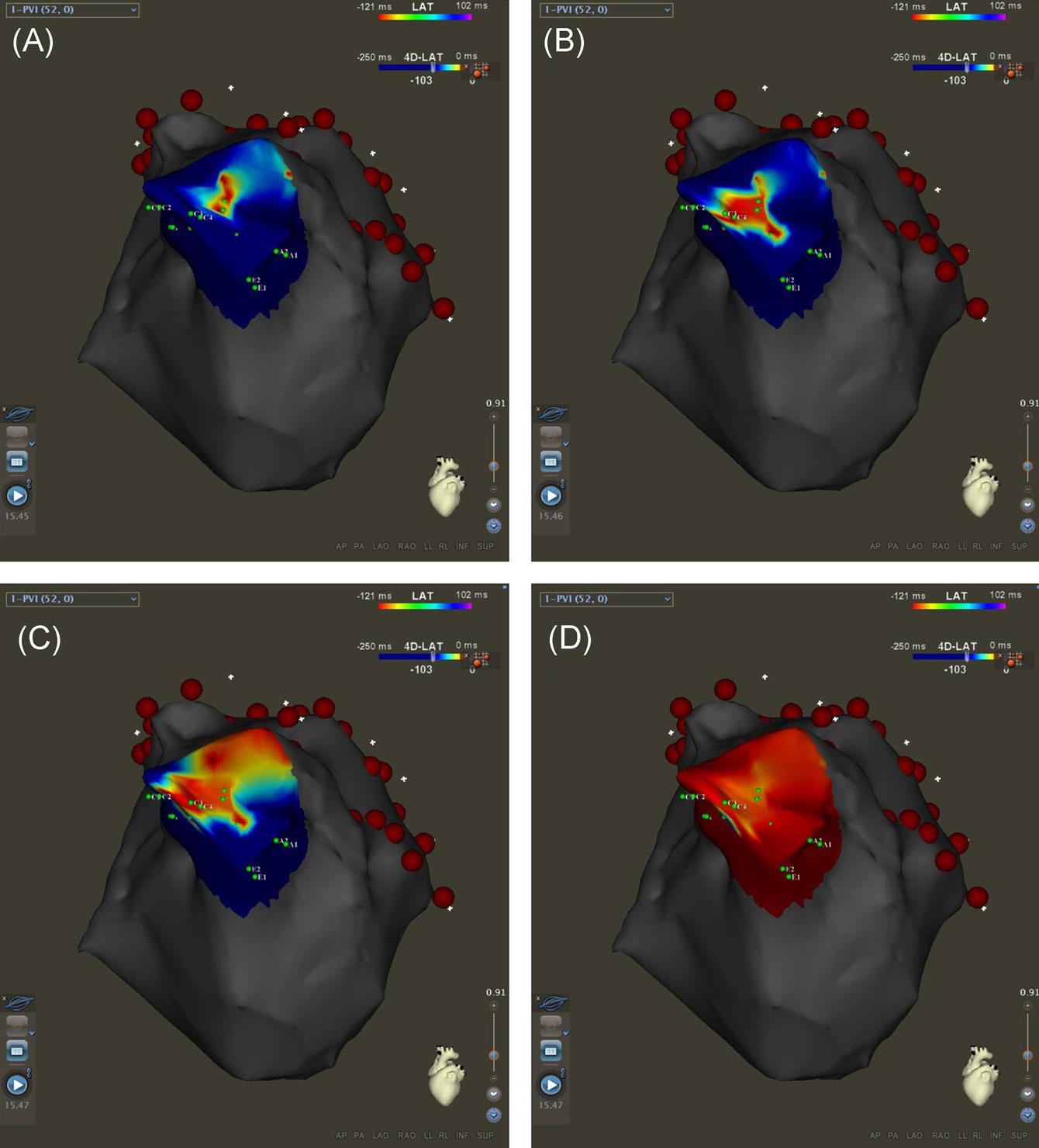
図2:CARTOFINDERによる心房細動中の興奮伝播様式の解析(文献2より)
また、肺静脈隔離後に再発した症例に対して2回目のアブレーションを行った際にもマッピングを行いましたが、1回目のアブレーションの際にみとめたfocal sourceとrotationのうち、それぞれ85%と63%が2回目のアブレーションの際にもみとめられ、focal sourceやrotationは肺静脈後の再発の原因となっており、それらをアブレーションすることにより治療成績が向上する可能性があることが示唆されました(図3、文献3)。以上の結果をふまえて、現在は、持続性心房細動に対して肺静脈隔離を施行後にCARTOFINDERをガイドにfocal sourceをアブレーションする術式と、肺静脈隔離単独の治療成績を比較する多施設無作為化研究を行っています。
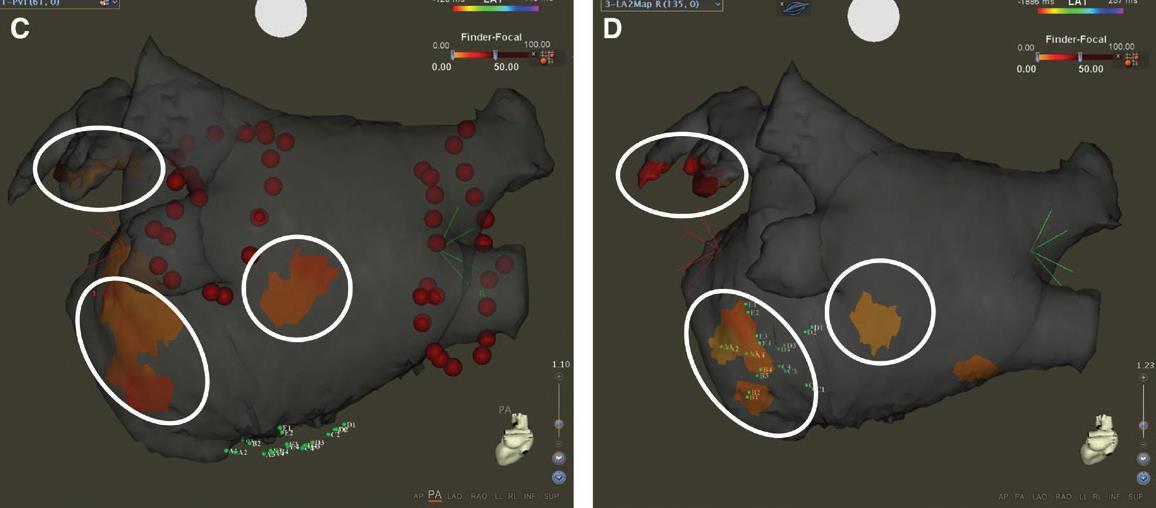
図3:CARTOFINDERによるfocal source部位の同定
オレンジ色がfocal source部位を示している。同一症例の1回目(左図)と2回目(右図)のアブレーション時の結果。
ほぼ同じ部位にfocal sourceがみとめられている。
・文献
- 1. Yamamoto T, Takahashi Y, Yamaguchi J, Sekigawa M, Shirai Y, Tao S, Hayashi T, Takigawa M, Goya M, Sasano T. Pulmonary vein narrowing after visually guided laser balloon ablation: Occurrence and clinical correlates. J Cardiovasc Electrophysiol. 2020 May 4. doi: 10.1111/jce.14525.
- 2. Takahashi Y, Akiyoshi K, Sekigawa M, Yagishita A, Yamamoto T, Maeda S, Kawabata M, Goya M, Hirao K, Sasano T. Endocardial contact mapping of the left atrial appendage in persistent atrial fibrillation. J Cardiovasc Electrophysiol. 2020 Jan;31(1):112-118.
- 3. Takahashi Y, Yamamoto T, Sekigawa M, Yamaguchi J, Shirai Y, Tao S, Hayashi T, Takigawa M, Goya M, Sasano T. Mapping After Pulmonary Vein Isolation in Persistent Atrial Fibrillation: Insights into the Role of Focal and Rotational Activation during Atrial Fibrillation. Circ Arrhythm Electrophysiol. 2020 Apr 17. doi: 10.1161/CIRCEP.120.008511.
カテーテルアブレーション②
心房頻拍、心室頻拍に対するカテーテルアブレーションに関する臨床研究
心房頻拍は複雑なリエントリー回路を有していることが多く、局所電位の解析や最新の3次元マッピングシステムを用いた解析が必要となることが多く経験されます。当科では3種類のマッピングシステム(CARTO, NaVx, Rhythmia)を用い研究を行っています。
心室頻拍は致死的となりうる不整脈です。当科は通常行われる心内膜側のアブレーションが無効の症例に対し、心外膜側アブレーション、外科とのHybridアブレーション、バイポーラー通電によるアブレーション、交感神経幹切除術等を積極的に行っています。
・文献
- 1. Yagishita A, Takahashi Y, Kawabata M, Kaneko M, Sekigawa M, Yamamoto T, Akiyoshi K, Shirai Y, Maeda S, Yamashita S, Suzuki M, Sasaki T, Goya M, Hirao K. Utility of a ripple map for the interpretation of atrial propagation during atrial tachycardia. J Interv Card Electrophysiol. 2019 Dec;56(3):249-257.
- 2. 滝川正晃 科学研究費基盤(C)20K17074 Omnipolar電位の周波数解析による局所電位選択の三次元マッピングへの応用
- 3. Yagishita A, Goya M, Takahashi Y, Ishibashi H, Akiyoshi K, Sekigawa M, Maeda S, Kawabata M, Okubo K, Hirao K. Bilateral cardiac sympathetic denervation of a recurrent refractory ventricular tachycardia occurring after catheter ablation of atrial fibrillation and outflow tract premature ventricular contractions. J Arrhythm. 2019 Jan 30;35(2):287-289.
植え込み型心臓デバイスリード抜去術に関する臨床研究
研究目的
植え込み型心臓デバイスリード抜去術は、デバイス植え込みポケット部感染症例やデバイス患者に生じた感染性心内膜炎症例にとって唯一無二の治療です。欧米に15年遅れ本邦に導入されたこともあり、国内で施行している施設数は多くありません。当科では心臓血管外科と連携し年間約60例に施行し、国内のトップランナーとなっています。 当科では最新の機器を導入し、より安全かつ確実なリード抜去手術の開発を目的とした臨床研究を行っています。
研究内容
<リード抜去術の適応>
植え込み型心臓デバイスリードは体内に留置後、時間経過とともに静脈壁や心内膜に癒着します。癒着したリードを抜去するためには、癒着を剥ぐための機器が必要となりますが、当科では主にエキシマレーザー・シースを用いています。レーザ―・シースを用いることにより、抜去の成功率は高くなりますが、レーザー・シースにより静脈や心内膜の損傷を引き起こして血胸や心タンポナーデを生じるリスクもあります。そのため、リードを抜去しないで保存的治療を継続した場合のリスクと、リード抜去術自体のリスクを考慮して適応が決定されます。感染症では、リード抜去せずに保存的治療を行う場合と、リードを含めた全システム抜去を施行した場合では、全システム抜去を施行した方が予後良好であることがこれまで示されているため、リード抜去が第一選択として行われています。
<リコール対象のリードの抜去術>
感染症例以外に、植え込み型除細動器(ICD)のショックリードに断線などの不具合が生じている場合も、リード抜去が必要となることがあります。不全ショックリードを使用していると、致死的不整脈を適切に除細動できなかったり、不整脈がないにもかかわらず除細動が行われたりすることがあります。不全ショックリードを抜去せずに、新しいリードが追加されることもありますが、ICDリードはペースメーカーリードよりも太いため、リード抜去せずに追加すると多くの症例で静脈の血栓性閉塞をきたし、上肢や顔面の浮腫や、さらなるリード追加ができなくなるためにCRTへのアップグレードができなくなることがあります。しかし、実臨床ではリード抜去術のリスクを恐れ、新しいリードの追加が行われることが多くの施設で現在も行われています。2000年代に販売されていた一部のICDリードは、植え込み後数年でリード不全が生じるためにリコール対象となったものもありました。このリコールリードが使用された患者に対して、リコールリードは抜去せずに、新しいリードが追加されることが多く、リコールリードの抜去術のデータはほとんどありませんでした(図1)。
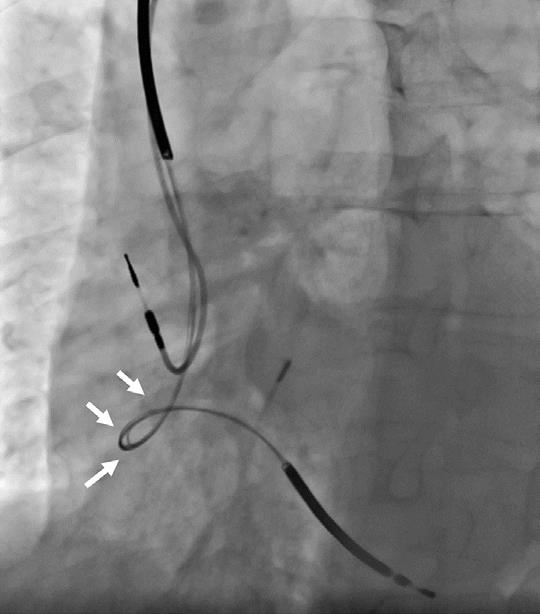
図1:導線露出したリコール対象の
ICDショックリード(文献1より)
そこで、当科は小倉記念病院との共同研究を行い、リコールICDリードの抜去術の治療成績をまとめて報告しています。28例にリード抜去術が行われましたが、全例でエキシマレーザー・シースが用いられ、1例で血胸のため外科的修復術を要しましたが、死亡例はなく、全例でリード抜去に成功しています (文献1)。この研究は、十分な症例数のある施設であれば、ICDショックリードの抜去術は比較的安全に施行することができることを本邦で初めて示した臨床研究であり、以後、リコール対象のICDリードのマネジメントの際に参考にされています。
<新しいエキシマレーザー・シースシステム>
エキシマレーザー・シースを用いても癒着を剥ぐことが困難な症例もあることから、エキシマレーザーの周波数を従来の40Hzから80Hzに変更されたものが2017年から使用できるようになりました。当科では80Hzのレーザー・シースを早期から導入し、65例に使用して、98%のリードの抜去に成功し、3.1%に合併症が生じたことを報告しています(文献2)。この研究で、実臨床において80Hzのレーザー・シースを用いても、合併症は増加しないことが確認されました。 <高齢者に対するリード抜去術> デバイス患者には高齢者が多いですが、高齢者は易感染性や皮膚の脆弱性のため、デバイス感染も多くみとめます。しかしながら、高齢患者に対するリード抜去術の治療成績はこれまで報告がないため、高齢患者のリード感染・リード不全症例に対しては保存的治療が選択される傾向がありました。そこで、高齢患者のリード抜去術の治療成績を当科より報告しています。当科でリード抜去術が施行された連続235例のうち、51例(22%)が80歳以上でした。80歳以上の患者では、リードの95%の抜去に成功し、重大な合併症は2.7%で、80歳以下の患者と成功率・合併症ともに有意差がなかったことを報告しています(図2、文献3)。以上のように、当科より報告した様々な治療成績報告は、リード抜去術の適応を決定する際の参考資料として役立っています。
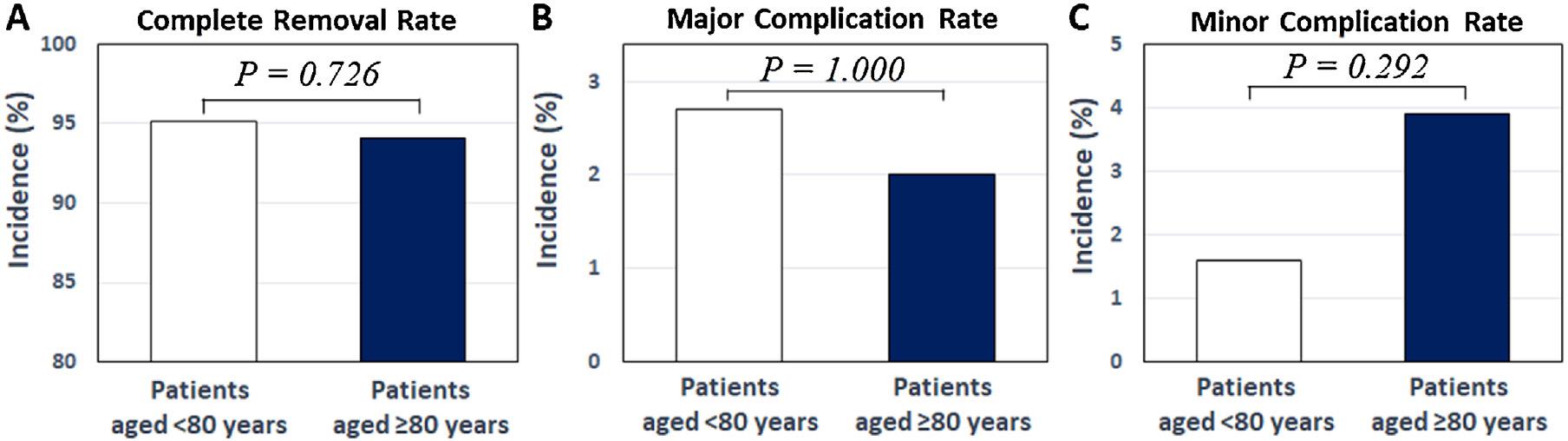
図2:リード抜去術の成功率と合併症:80歳以上と以下の症例の比較(文献3より)
・文献
- Goya M, Nagashima M, Hiroshima KI, Hayashi K, Makihara Y, Fukunaga M, An Y, Ohe M, Sasaki T, Shiohira S, Shirai Y, Kawabata M, Ando K, Isobe M, Hirao K. Transvenous extraction of advisory implantable cardioverter defibrillator leads with a relatively long implant duration. J Cardiol. 2018 Oct;72(4):316-320.
- Yoshitake T, Goya M, Sasaki T, Shiohira S, Sekigawa M, Shirai Y, Lee K, Yagishita A, Maeda S, Takahashi Y, Kawabata M, Hirao K. Safety and Efficacy of Transvenous Lead Extraction With a High-Frequency Excimer Laser – A Single Center Experience. Circ J. 2018 Nov 24;82(12):2992-2997.
- Yagishita A, Goya M, Sekigawa M, Yamamoto T, Akiyoshi K, Maeda S, Takahashi Y, Kawabata M, Hirao K. Transvenous excimer laser-assisted lead extraction of cardiac implantable electrical devices in the Japanese elderly population. J Cardiol. 2020 Apr;75(4):410-414.
文:合屋雅彦、高橋良英





